Joissain tarinan versioissa kerrotaan, että tapaturman takana oli mustasukkaisen tuulen jumala Zefyr(os)in aiheuttama äkillinen puhuri – tämä kun tavoitteli myös komean nuorukaisen huomiota.
Olipa tragedian syy mikä tahansa, Apollo ei halunnut kumppaniaan Manalaan, vaan loihti tämän verestä kukan, jonka terälehdille vielä vieritti kyyneleen muistoksi surustaan.
Tarussa syntynyt kukka tosin taisi olla ihan muu kuin nykyisin tuntemamme hyasintti. Nykytietämys veikkaa sen olleen kurjenmiekka, pikkusinililja tai jokin vastaava. Linné virallisti nyky-hyasintin nimen vuonna 1753. Kukka oli nimetty Hyakinthoksen muistoksi jo aiemmin.
Hyasintti (Hyacinthus orientalis) on Suomessa ja muuallakin länsimaissa suosittu joulukukka. Myös helmililjoja ja paria muutakin kasvisukua kutsutaan ulkomuotonsa vuoksi erheellisesti joskus (marja- tai rypäle)hyasinteiksi.
Hyasintti on alunperin kotoisin Lähi-idän pohjois- ja itäosista. Nykyään sitä viljellään laajalti koristekasvina.
Hyasintin sipulit ovat oksaalihapponsa vuoksi hieman myrkyllisiä. Vaikka aine on eräs voimakkaimmista orgaanisista hapoista, se aiheuttaa todellisia ongelmia vain nieltynä. Hyasintin sipulien normaalista käsittelystä voi saada enintään iho-oireita.
Allergikot ovat usein hyvin herkkiä hyasintin hajulle.
Hyasintissa huomioitavaa on myös sen varsin voimakas tuoksu. Joidenkin mielestä se on oikeaa joulun tuoksua kuusen odöörin kanssa, mutta toiset taas kiikuttavat kukat saman tien ulos tai parvekkeelle.
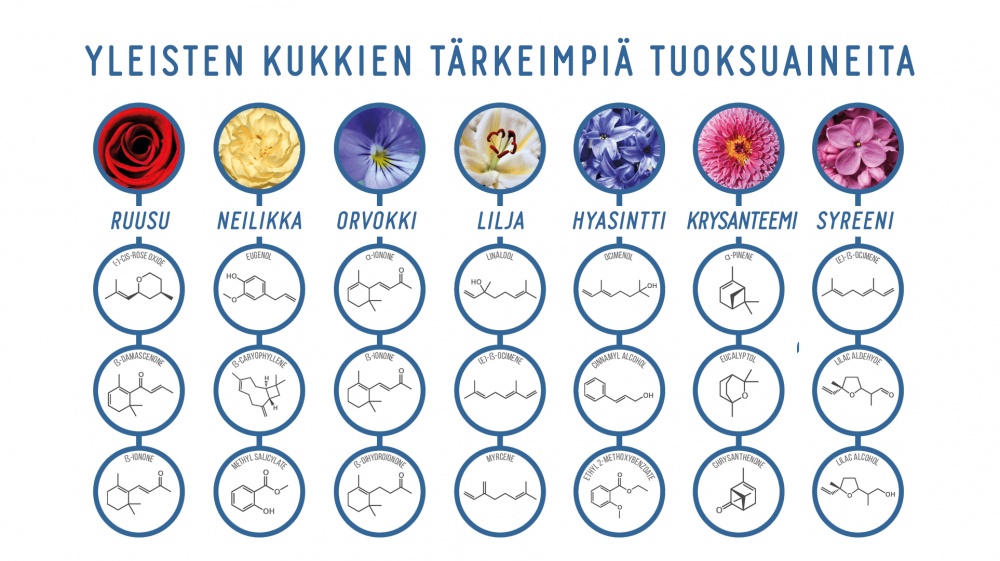
Mistä tulevat hyasintin ja muiden kukkien tuoksut?
Vähemmän yllättäen tässäkin on takana kemia ja varsin monimutkainen kemian osa-alue: tuoksujen ja aromien kemia. Aromi ei ole koskaan vain yhdestä aineesta kiinni, vaan maut ja hajut ovat aina useiden aineiden yhteisvaikutuksia, jotka jokainen maistaa ja haistaa hieman eri tavalla.
Kukat tuottavat voimakkaita aromeja, koska ne haluavat houkutella hyönteisiä luokseen. Voisi sanoa, että niiden tarkoituksena onkin olla kauniita ja tuoksuvia, ja juuri siksi ne sopivat erityisen hyvin koristeluun.
Vaikka aromit koostuvatkin lukuisista (yleensä) orgaanisista yhdisteistä, on kullakin kukkatyypillä muutamia niille luonteenomaisia aineita.